 Персональный сайт учителя химии Кардаевой Татьяны Александровны
Персональный сайт учителя химии Кардаевой Татьяны Александровны
ХИМИЯ – это область чудес, в ней скрыто счастье человечества,
величайшие завоевания разума будут сделаны
именно в этой области.(М. ГОРЬКИЙ)
Таблица
|
Фенол
Фенолы - производные ароматических углеводородов, в молекулах которых гидроксильная группа (- ОН) непосредственно связана с атомами углерода в бензольном кольце.
I. Классификация фенолов
Различают одно-, двух-, трехатомные фенолы в зависимости от количества ОН-групп в молекуле:
В соответствии с количеством конденсированных ароматических циклов в молекуле различают сами фенолы (одно ароматическое ядро – производные бензола), нафтолы (2 конденсированных ядра – производные нафталина), антранолы (3 конденсированных ядра – производные антрацена) и фенантролы:
II. Изомерия и номенклатура фенолов
Возможны 2 типа изомерии
1. Изомерия положения заместителей в бензольном кольце

2. Изомерия боковой цепи (строения алкильного радикала и числа радикалов)
Для фенолов широко используют тривиальные названия, сложившиеся исторически. В названиях замещенных моноядерных фенолов используются также приставки орто-, мета-и пара -, употребляемые в номенклатуре ароматических соединений. Для более сложных соединений нумеруют атомы, входящие в состав ароматических циклов и с помощью цифровых индексов указывают положение заместителей
III. Строение молекулы

Фенильная группа C6H5 – и гидроксил –ОН взаимно влияют друг на друга
Неподеленная электронная пара атома кислорода притягивается 6-ти электронным облаком бензольного кольца, из – за чего связь О–Н еще сильнее поляризуется. Фенол - более сильная кислота, чем вода и спирты.
В бензольном кольце нарушается симметричность электронного облака, электронная плотность повышается в положении 2, 4, 6. Это делает более реакционноспособными связи С-Н в положениях 2, 4, 6. и – связи бензольного кольца.
Взаимное влияние атомов в молекуле фенола
IV. Физические свойства
Видео-опыт: “Изучение физических свойств фенола”
Большинство одноатомных фенолов при нормальных условиях представляют собой бесцветные кристаллические вещества с невысокой температурой плавления и характерным запахом. Фенолы малорастворимы в воде, хорошо растворяются в органических растворителях, токсичны, при хранении на воздухе постепенно темнеют в результате окисления.
Фенол C6H5OH (карболовая кислота) — бесцветное кристаллическое вещество на воздухе окисляется и становится розовым, при обычной температуре ограниченно растворим в воде, выше 66 °C смешивается с водой в любых соотношениях. Фенол — токсичное вещество, вызывает ожоги кожи, является антисептиком
V. Токсические свойства
Фенол ядовит. Вызывает нарушение функций нервной системы. Пыль, пары и раствор фенола раздражают слизистые оболочки глаз, дыхательных путей, кожу. Попадая в организм, Фенол очень быстро всасывается даже через неповрежденные участки кожи и уже через несколько минут начинает воздействовать на ткани головного мозга. Сначала возникает кратковременное возбуждение, а потом и паралич дыхательного центра. Даже при воздействии минимальных доз фенола наблюдается чихание, кашель, головная боль, головокружение, бледность, тошнота, упадок сил. Тяжелые случаи отравления характеризуются бессознательным состоянием, синюхой, затруднением дыхания, нечувствительностью роговицы, скорым, едва ощутимым пульсом, холодным потом, нередко судорогами. Зачастую фенол является причиной онкозаболеваний.
VI. Применение фенолов
1. Производство синтетических смол, пластмасс, полиамидов
2. Лекарственных препаратов
3. Красителей
4. Поверхностно-активных веществ
5. Антиоксидантов
6. Антисептиков
7. Взрывчатых веществ
VII. Получение фенола в промышленности
1. Кумольный способ
(СССР, Сергеев П.Г., Удрис Р.Ю., Кружалов Б.Д., 1949 г.). Преимущества метода: безотходная технология (выход полезных продуктов > 99%) и экономичность. В настоящее время кумольный способ используется как основной в мировом производстве фенола.
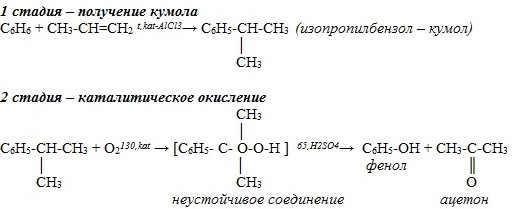
2. Из каменноугольной смолы (как побочный продукт – выход мал):
C6H5ONa + H2SO4(разб) → С6H5 – OH + NaHSO4
фенолят натрия
(продукт обработки смолы едким натром)
3. Из галогенбензолов
С6H5-Cl + NaOH t,p → С6H5 – OH + NaCl
4. Сплавлением солей ароматических сульфокислот с твёрдыми щелочами
C6H5-SO3Na + NaOH t → Na2SO3 + С6H5 – OH
натриевая соль
бензолсульфокислоты
VIII. Химические свойства фенола (карболовой кислоты)
1. Реакции, идущие по гидроксильной группе
Кислотные свойства – выражены ярче, чем у предельных спиртов (окраску индикаторов не меняют):
1) С активными металлами: 2C6H5-OH + 2Na → 2C6H5-ONa + H2
фенолят натрия
Видео-опыт: “Взаимодействие фенола с металлическим натрием”
2) Со щелочами: C6H5-OH + NaOH (водн. р-р) ↔ C6H5-ONa + H2O
Видео-опыт: “Взаимодействие фенола с раствором щелочи”
! Феноляты – соли слабой карболовой кислоты, разлагаются угольной кислотой –
C6H5-ONa + H2O + СO2 → C6H5-OH + NaHCO3
По кислотным свойствам фенол превосходит этанол в 106 раз. При этом во столько же раз уступает уксусной кислоте. В отличие от карбоновых кислот, фенол не может вытеснить угольную кислоту из её солей
C6H5-OH + NaHCO3 = реакция не идёт – прекрасно растворяясь в водных растворах щелочей, он фактически не растворяется в водном растворе гидрокарбоната натрия.
Кислотные свойства фенола усиливаются под влиянием связанных с бензольным кольцом электроноакцепторных групп (NO2-, Br-)
C6H5-OH< п-нитрофенол < 2,4,6-тринитрофенол
2,4,6-тринитрофенол или пикриновая кислота сильнее угольной
2. Реакции, идущие по бензольному кольцу
Взаимное влияние атомов в молекуле фенола проявляется не только в особенностях поведения гидроксигруппы (см. выше), но и в большей реакционной способности бензольного ядра. Гидроксильная группа повышает электронную плотность в бензольном кольце, особенно, в орто- и пара-положениях (+М-эффект ОН-группы):

Поэтому фенол значительно активнее бензола вступает в реакции электрофильного замещения в ароматическом кольце.
1) Нитрование
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов:

При использовании концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота):

2) Галогенирование
Фенол легко при комнатной температуре взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол):

3) Конденсация с альдегидами
4) Гидрирование фенола
C6H5-OH + 3H2 Ni, 170ºC → C6H11 – OH циклогексиловый спирт (циклогексанол)
3. Качественная реакция - обнаружение фенола
Видео-опыт: “Качественная реакция на фенол”
6C6H5-OH + FeCl3 → [Fe(C6H5-OH)3](C6H5O)3 + 3HCl
FeCl3 - светло-жёлтый раствор
[Fe(C6H5-OH)3](C6H5O)3 - фиолетовый раствор
IX. Тренажеры
Тренажер №1:“Физические свойства фенола”
Тренажер №2:“Химические свойства фенола”
Тестовые задания по теме "Фенолы"
ЦОРы
Видео-опыт: “Изучение физических свойств фенола”
Видео-опыт: “Взаимодействие фенола с металлическим натрием”
Видео-опыт: “Взаимодействие фенола с раствором щелочи”
Видео-опыт: “Взаимодействие фенола с бромной водой”
Видео-опыт: “Качественная реакция на фенол”






