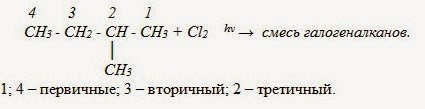Персональный сайт учителя химии Кардаевой Татьяны Александровны
Персональный сайт учителя химии Кардаевой Татьяны Александровны
ХИМИЯ – это область чудес, в ней скрыто счастье человечества,
величайшие завоевания разума будут сделаны
именно в этой области.(М. ГОРЬКИЙ)
Таблица
|
Алканы: физические и химические свойства, получение и применение
I. Физические свойства
В обычных условиях
С1- С4 – газы
С5- С15 – жидкие
С16 – твёрдые
Температуры плавления и кипения алканов, их плотности увеличиваются в гомологическом ряду с ростом молекулярной массы. Все алканы легче воды, в ней не растворимы, однако растворимы в неполярных растворителях (например, в бензоле) и сами являются хорошими растворителями. Физические свойства некоторых алканов представлены в таблице.
Таблица 2. Физические свойства некоторых алканов
|
Название |
Формула |
tпл °С |
tкип °С |
|
Метан |
СН4 |
-182,5 |
-161,5 |
|
Этан |
С2Н6 |
-182,8 |
-88,6 |
|
Пропан |
С3Н8 |
-187,7 |
-42 |
|
Бутан |
С4Н10 |
-138,3 |
-0,5 |
|
Пентан |
C5H12 |
-129,7 |
+36,1 |
|
Гексан |
С6Н14 |
-95,3 |
68,7 |
|
Гептан |
С7H16 |
-90,6 |
98,4 |
|
Октан |
C8H18 |
-56,8 |
124,7 |
|
Нонан |
С9Н20 |
-53,7 |
150,8 |
|
Декан |
C10H22 |
-29,6 |
174,0 |
|
Пентадекан |
C15H32 |
+10 |
270,6 |
|
Эйкозан |
С20Н42 |
36,8 |
342,7 |
|
Пентакозан |
C25H52 |
53,7 |
400 |
II. Химические свойства алканов
1. Реакции замещения
а) Галогенирование
При действии света - hν или нагревании (стадийно – замещение атомов водорода на галоген носит последовательный цепной характер. Большой вклад в разработку цепных реакций внёс физик, академик, лауреат Нобелевской премии Н. Н. Семёнов )
В реакции образуются вещества галогеналканы RГ или Сn H2n+1Г
(Г - это галогены F, Cl, Br, I)
CH4 + Cl2 hν → CH3Cl + HCl (1 стадия)
метан хлорметан
CH3Cl + Cl2 hν → CH2Cl2 + HCl (2 стадия)
дихлорметан
СH2Cl2 + Cl2 hν → CHCl3 + HCl (3 стадия)
трихлорметан
CHCl3 + Cl2 hν → CCl4 + HCl (4 стадия)
тетрахлорметан
Скорость реакции замещения водорода на атом галогена у галогеналканов выше, чем у соответствующего алкана, это связано с взаимным влиянием атомов в молекуле:
Электронная плотность связи С – Cl смещена к более электроотрицательному хлору, в результате на нём скапливается частичный отрицательный заряд, а на атоме углерода – частичный положительный заряд.
На атом углерода в метильной группе ( - СН3) создаётся дефицит электронной плотности, поэтому он компенсирует свой заряд за счёт соседних атомов водорода, в результате связь С – Н становится менее прочной и атомы водорода легче замещаются на атомы хлора. При увеличении углеводородного радикала наиболее подвижными остаются атомы водорода у атома углерода ближайщего к заместителю:
CH3 – CH2 – Cl + Cl2 hν → CH3 – CHCl2 + HCl
хлорэтан 1,1 -дихлорэтан
Со фтором реакция идёт со взрывом.
С хлором и бромом требуется инициатор.
Иодирование происходит обратимо, поэтому требуется окислитель для удаления HI из рекции.
Внимание!
В реакциях замещения алканов легче всего замещаются атомы водорода у третичных атомов углерода, затем у вторичных и, в последнюю очередь, у первичных. Для хлорирования эта закономерность не соблюдается при T>400˚C.
б) Нитрование (реакция М.И. Коновалова, он провёл её впервые в 1888 г)
CH4 + HNO3 (раствор) t˚С → CH3NO2 + H2O
нитрометан
RNO2 или Сn H2n+1 NO2 (нитроалкан)
2. Реакции отщепления (дегидрирование)
а) CnH2n+2 t˚С, Ni или Pd → CnH2n + H2
б) При нагревании до 1500 С происходит образование ацетилена и водорода:
2CH4 1500°С → C2H2 + 3H2
3. Реакции перегруппировки (изомеризация)
н-алкан AlCl3, t°С → изоалкан
Анимация: “Реакция изомеризации”
4. Реакции горения (горят светлым не коптящим пламенем)
CnH2n+2 + O2 t°С → nCO2 + (n+1)H2O
Помните! Смесь метана с воздухом и кислородом взрывоопасна
V(CH4) : V(O2) = 1: 2
V(CH4) : V(воздуха) = 1 : 10
Видео: “Взрыв метана с кислородом”
Видео: “Горение парафина в условиях избытка и недостатка кислорода”
Видео: “Горение метана и изучение его физических свойств”
Видео: “Горение жидких углеводородов”
Видео: “Горение твердых углеводородов (на примере парафина)”
5. Реакции разложения
а) Крекинг при температуре 700-1000°С разрываются (-С-С-) связи:
C10H22 t°С → C5H12 + C5H10
алкан алкен
Анимация: “Термическое разложение алканов (крекинг)”
б) Пиролиз при температуре 1000°С разрываются все связи,
продукты – С и Н2:
СH4 1000°С → C + 2H2
в) Конверсия метана с образованием синтез – газа (СО + Н2)
CH4 + H2O 800˚C, Ni → СО + 3Н2
III. Получение алканов
1. Получение в лаборатории
1. Гидролиз карбида алюминия (получение метана):
Al4C3 + 12H2O = 4Al(OH)3 + 3CH4↑
2. Реакция Вюрца (взаимодействие натрия с галогенпроизводными алканов):
R-Г + 2Na + Г-R1 → R-R1 + 2NaГ
(R- это радикал; Г- это галоген)
a) CH3-Cl + 2Na + Cl-CH3 → CH3-CH3 + 2NaCl
или
2CH3Cl + 2Na → C2H6 + 2NaCl
б) CH3-I + 2Na + I-C2H5 → CH3-C2H5 + 2NaI
или
CH3I + 2Na + C2H5I → C3H8 + 2NaI
3. Термическое декарбоксилирование солей карбоновых кислот в присутствии щелочей:
Видео: “Получение метана”
R-COONa + NaOH -t ˚С→ R-H + Na2CO3
a) CH3-COONa + NaOH -t ˚С→ CH4 + Na2CO3
(ацетат натрия+ едкий натр=(метан+карбонат натрия)
б) C2H5-COONa + NaOH -t ˚С→ C2H6 + Na2CO3
этилат натрия этан
4. Каталитическое гидрирование алкенов и алкинов:
a) CnH2n + H2 -t,kat,p → CnH2n+2
алкен
C2H4 + H2 -300°C,Ni → C2H6
б) CnH2n-2 + 2H2 - t,kat→ CnH2n+2
алкин
C2H2 + 2H2 - t,kat→ C2H6
5. Электролиз растворов солей карбоновых кислот - реакция КОЛЬБЕ
Пример. Электролиз водного раствора ацетата натрия
H2O, CH3COONa ↔ Na+ + CH3COO-
Катод (-): H2O, Na+ - Процесс восстановления: 2H2O + 2ē → H2↑ + 2OH-
Анод (+): H2O, CH3COO-(анионы органических кислот активнее воды) – Процесс окисления:
CH3COO- -1e-→ CH3COO∙ (радикал)
CH3COO∙ → CH3∙ + СО2↑
2СН3 ∙ → С2Н6
Итог:
2H2O + 2CH3COONa эл.ток= H2 + 2CO2 + 2NaOH + C2H6
2H2O + 2CH3COONa эл.ток= H2 + 2NaHCO3 + C2H6
2. Получение в промышленности
1. Из природного и попутного нефтяного газа
Важнейшим источником алканов в природе является природный газ, минеральное углеводородное сырье - нефть и сопутствующие ей нефтяные газы. Природный газ на 95 процентов состоит из метана. Такой же состав имеет болотный газ, образующийся в результате переработки бактериями (гниения) углеводов.
Метан называют ещё и болотным; рудничным газом.
Попутные нефтяные газы состоят в основном из этана, пропана, бутана и частично пентана. Их отделяют от нефти на специальных установках по подготовке нефти. При отсутствии газоконденсатных станций попутные нефтяные газы сжигают в факелах, что является крайне неразумной и разорительной практикой в нефтедобыче. Одновременно с газами нефть очищается от воды, грязи и песка, после чего поступает в трубу для транспортировки. Из нефти при ее разгонке (перегонке, дистилляции) отбирая последовательно все более и более высококипящие фракции получают:
бензины - т. кип. от 40 до 180 С, (содержит углеводороды С5-С10), состоит более, чем из 100 индивидуальных соединений, нормальных и разветвленных алканов, циклоалканов, алкенов и ароматических углеводородов;
керосин 180-230 C, (С11-С12);
легкий газойль (дизельное топливо) 230-305 С (С13-С17);
тяжелый газойль и легкий дистиллят смазочного масла 305-405 С (С18-С25);
смазочные масла 405-515 С (С26-С38).
Остаток после перегонки нефти называется асфальтом или битумом.
2. Синтезом из водяного газа:
nCO + (2n + 1) H2 - t,kat→ CnH2n+2 + n H2O
CO + 3H2 - t,kat→ CH4 + H2O
3. Синтезом из простых веществ:
nC + (n + 1) H2 -t,kat,p → CnH2n+2
C + 2 H2 - 500°C,Ni → CH4
IV. Применение
1. Предельные углеводороды находят широкое применение в самых разнообразных сферах жизни и деятельности человека.
2. Использование в качестве топлива – в котельных установках, бензин, дизельное топливо, авиационное топливо, баллоны с пропан-бутановой смесью для бытовых плит.
3. Вазелин используется в медицине, парфюмерии, косметике, высшие алканы входят в состав смазочных масел, соединения алканов применяются в качестве хладагентов в домашних холодильниках.
4. Смесь изомерных пентанов и гексанов называется петролейным эфиром и применяется в качестве растворителя. Циклогексан также широко применяется в качестве растворителя и для синтеза полимеров.
5. Метан используется для производства шин и краски.
6. Значение алканов в современном мире огромно. В нефтехимической промышленности предельные улеводороды являются базой для получения разнообразных органических соединений, важным сырьем в процессах получения полупродуктов для производства пластмасс, каучуков, синтетических волокон, моющих средств и многих других веществ. Велико значение в медицине, парфюмерии и косметике.
Использование алканов в качестве смазочных материалов
Использование алканов в качестве топлива
Использование парафина для получения водостойкой бумаги
Применение алканов в медицине (вазелин, парафин и др.)
Применение галогенопроизводных алканов
V. Тренажёры
Тренажер №1: “Алканы: строение, номенклатура, получение и физические свойства”
Тренажер №2: “Алканы: строение, номенклатура, получение и физические свойства (расчетные задачи)”
Тренажер №3: “Определение качественного состава парафина по продуктам окисления”
Тренажер №4: “Химические свойства алканов”
ЦОРы
Анимация:“Реакция изомеризации”
Анимация:“Термическое разложение алканов (крекинг)”
Видео: “Горение парафина в условиях избытка и недостатка кислорода”
Видео:“Горение метана и изучение его физических свойств”
Видео:“Горение жидких углеводородов”
Видео: “Горение твердых углеводородов (на примере парафина)”
Видео: “Установление качественного состава предельных углеводородов”
Видео: “Определение содержания хлора в органических соединениях”
Видео: “Отношение метана к раствору перманганата калия и бромной воде”
Видео: “Взрыв метана с кислородом”
Видео: “Получение метана”