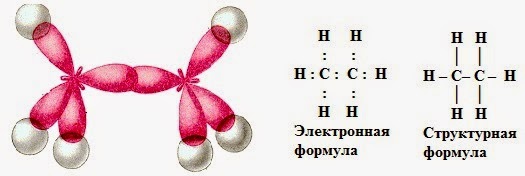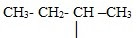Персональный сайт учителя химии Кардаевой Татьяны Александровны
Персональный сайт учителя химии Кардаевой Татьяны Александровны
ХИМИЯ – это область чудес, в ней скрыто счастье человечества,
величайшие завоевания разума будут сделаны
именно в этой области.(М. ГОРЬКИЙ)
Таблица
|
Алканы: электронное и пространственное строение, гомологи и изомеры, номенклатура
I. Видеоурок: “Алканы”
II. Гомологический ряд алканов
Алканы (предельные углеводороды) – это алифатические (ациклические), насыщенные углеводороды, в которых все валентности атомов углерода, не затраченные на образование простых С – С связей, насыщены атомами водорода.
Общая формула алканов – СnH2n+2
В таблице представлены некоторые представители ряда алканов и их радикалы.
|
Формула |
Название |
Название радикала |
|
CH4 |
метан |
- CH3 метил |
|
C2H6 |
этан |
- C2H5 этил |
|
C3H8 |
пропан |
- C3H7 пропил |
|
C4H10 |
бутан |
- C4H9 бутил |
|
C4H10 |
изобутан |
изобутил |
|
C5H12 |
пентан |
пентил |
|
C5H12 |
изопентан |
изопентил |
|
C5H12 |
неопентан |
неопентил |
|
C6H14 |
гексан |
гексил |
|
C7H16 |
гептан |
гептил |
|
C10H22 |
декан |
децил |
Из таблицы видно, что эти углеводороды отличаются друг от друга количеством групп - СН2 -.Такой ряд сходных по строению, обладающих близкими химическими свойствами и отличающихся друг от друга числом данных групп называется гомологическим рядом. А вещества, составляющие его называются гомологами.
Гомологи – вещества сходные по строению и свойствам, но отличающиеся по составу на одну или несколько гомологических разностей (- СН2 -).
Тренажёр: "Гомологический ряд алканов"
III. Строение алканов
Основные характеристики:
- пространственное строение – тетраэдрическое
- sp3 – гибридизация,
- ‹ HCH = 109 ° 28
- Углеродная цепь - зигзаг (если n ≥ 3)
- σ – связи (свободное вращение вокруг связей)
- длина (-С-С-) 0,154 нм
- энергия связи (-С-С-) 348 кДж/моль
Все атомы углерода в молекулах алканов находятся в состоянии sр3-гибридизации
Угол между связями С-C составляет 109°28', поэтому молекулы нормальных алканов с большим числом атомов углерода имеют зигзагообразное строение (зигзаг). Длина связи С-С в предельных углеводородах равна 0,154 нм (1нм=1*10-9м).
Анимация: “Образование молекулы метана”
а) электронная и структурная формулы
б) пространственное строение
Строение молекулы этана С2Н6
Строение молекулы пропана С3Н8 – цепь зигзагообразная
Тренажёр: "Состав и строение алканов"
IV. Изомерия алканов
Характерна СТРУКТУРНАЯ изомерия цепи с С4
Один из этих изомеров (н-бутан) содержит неразветвленную углеродную цепь, а другой — изобутан — разветвленную (изостроение).
Атомы углерода в разветвленной цепи различаются типом соединения с другими углеродными атомами. Так, атом углерода, связанный только с одном другим углеродным атомом, называется первичным, с двумя другими атомами углерода – вторичным, с тремя – третичным, с четырьмя – четвертичным.
С увеличением числа атомов углерода в составе молекул увеличиваются возможности для разветвления цепи, т.е. количество изомеров растет с ростом числа углеродных атомов.
Сравнительная характеристика гомологов и изомеров
V. Номенклатура алканов
Свою номенклатуру имеют радикалы (углеводородные радикалы)
Число одинаковых заместителей указывают при помощи множительных приставок:
- два – «ди»
- три – «три»
- четыре – «тетра»
- пять – «пента»
- шесть – «гекса»
- семь – «гепта»
- восемь – «окта»
- девять – «нано»
Для названия предельных углеводородов применяют в основном систематическую (международная номенклатура IUPAC) и рациональную номенклатуры.
1. Рациональная номенклатура
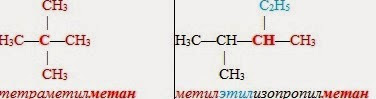
По рациональной номенклатуре алканы рассматривают как производные простейшего углеводорода — метана, в молекуле которого один или несколько водородных атомов замещены на радикалы. Эти заместители (радикалы) называют по старшинству (от менее сложных к более сложным). Если эти заместители одинаковые, то указывают их количество. В основу названия включают слово "метан":
2. Систематическая номенклатура
Правила систематической номенклатуры:
1. В формуле молекулы алкана выбираем главную цепь — самую длинную.
2. Затем эту цепь нумеруем с того конца, к которому ближе расположен заместитель (радикал). (Если заместителей несколько, то поступают так, чтобы цифры, указывающие их положение, были наименьшими) Заместители перечисляем по алфавиту.
Таким образом, углеводород может быть назван: 2 - метил - 4 - этилгептан (но не 6-метил-4-этилгептан).
Анимация: “Образование названий алканов по номенклатуре ИЮПАК”
Анимация: “Примеры разной записи формул одного и того же вещества”
Тренажер №1: “Первичные, вторичные и третичные атомы углерода”
Тренажер №2: “Составление формул алканов по названию”
ЦОРы
Видеоурок:“Алканы”
Анимация: “Образование молекулы метана”
Анимация: “Образование названий алканов по номенклатуре ИЮПАК”
Анимация: “Примеры разной записи формул одного и того же вещества”